2025.05.16
治療を逃れる白血病幹細胞の「隠れ家」とは? ~白血病再発の原因となる白血病幹細胞の潜伏場所と生存戦略の解明~ (幹細胞再生修復医学分野/がん幹細胞医学分野 新井 文用教授、八尾 尚幸助教)
ポイント
概要
急性骨髄性白血病 (AML)*7の治療において、完全寛解*8後の再発は大きな課題となっています。この再発の主な原因の一つが白血病幹細胞 (LSC) の存在です。白血病幹細胞は従来の化学療法に対して高い抵抗性を持ち、治療後も骨髄内に微小残存病変として生存することが明らかになっています。注目すべき点は、白血病幹細胞がニッチと呼ばれる骨髄の微小環境に留まり、細胞周期を静止状態にすることで抗がん薬の作用を回避する特性を持つことです。この白血病幹細胞の特性により、患者が完全寛解に達した後でも、白血病幹細胞が再び活性化して白血病細胞の増殖を引き起こし、再発に至ることがあります。したがって、急性骨髄性白血病の根治的治療を実現するためには、白血病幹細胞とその白血病ニッチを標的とした革新的な治療戦略の確立が必要です。
九州大学大学院医学研究院の新井文用教授、八尾尚幸助教、Ngan Thi Kim Nguyen 大学院生らの研究グループは、白血病幹細胞が潜む白血病ニッチについて着目して白血病マウスモデルの解析を行い、骨内膜ニッチに存在する Alcam 陽性の骨ライニング細胞 (Alcam+ BLC) が、白血病幹細胞を治療抵抗性の「静止状態」に維持する重要な役割を果たしていることを明らかにしました。細胞周期が静止期にある白血病幹細胞は、Alcam+ BLC が豊富な領域に集積していました。さらに、白血病幹細胞から分泌される TGF-β1 が Alcam+ BLC のオステオポンチン (OPN) 産生を促進し、分泌されたオステオポンチンが白血病幹細胞を骨内膜ニッチに留め、静止状態を維持するという TGF-β1/Tgfbr2/OPN シグナル経路を同定しました。これらの知見は、従来の化学療法では排除が困難であった静止期白血病幹細胞を標的とした治療薬開発が可能になると期待されます。
本研究成果は、Nature Publishing Groupの Leukemia 誌に2025年5月13日 (火) (日本時間) に掲載されました。
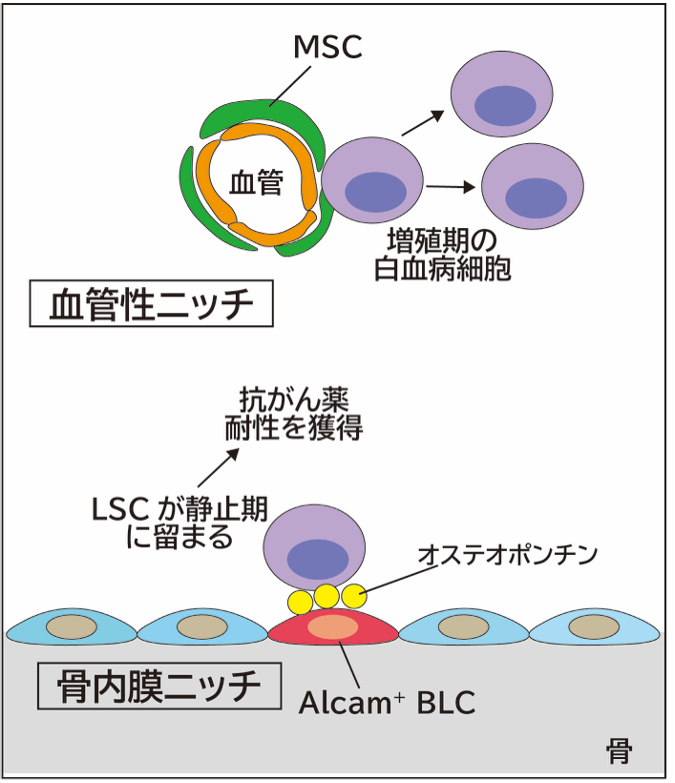
図:本研究の概要
骨内膜ニッチと血管性ニッチは白血病幹細胞 (LSC) に対してそれぞれ異なる役割を担っています。骨内膜ニッチは白血病幹細胞の静止状態維持に重要な役割を果たしています。一方、血管性ニッチでは白血病幹細胞の活性化と増殖を支持しています。
研究者からひとこと
本研究成果は、白血病幹細胞の治療抵抗性メカニズムの解明において重要な前進をもたらしました。特に、TGF-β1/Tgfbr2/OPN シグナル経路の同定は、従来の化学療法では効果が限定的であった静止期白血病幹細胞を標的とする革新的な治療アプローチの開発に直接つながる発見だと考えています。
研究の背景
急性骨髄性白血病においては、完全寛解に至った後も再発が依然として大きな課題となっています。再発の原因の一つは、正常な造血幹細胞 (HSC)*9と同様の自己複製能を持ち、白血病細胞を産生する白血病幹細胞の存在です。白血病幹細胞は一般的な化学療法に対して高い抵抗性を示し、治療後も骨髄内に微小残存病変として潜伏し続けることが明らかにされています。白血病幹細胞は、造血幹細胞と同様に、骨髄内の特殊な微小環境である「ニッチ」に存在しており、ニッチは複雑なシグナルネットワークを通じてその機能を制御しています。特に重要なことは、白血病幹細胞がニッチに留まり、細胞周期を静止状態に保つことで、抗がん剤の影響を回避する性質を持つ点です。このため、臨床的には完全寛解と判断された場合でも、白血病幹細胞が再び活性化されることで白血病細胞の増殖が再開され、結果として再発に至る可能性があります。このような背景から、急性骨髄性白血病を根本的に治癒するためには、白血病幹細胞そのものだけでなく、それを維持や保護する白血病ニッチも同時に標的とした新たな治療戦略の開発が不可欠であると考えられています。
骨髄ニッチは、血管周囲の「血管性ニッチ」と骨表面の「骨内膜ニッチ」に分類されます。血管性ニッチは間葉系幹細胞(MSC)*10や内皮細胞などで構成され、骨内膜ニッチは骨芽細胞や間葉系幹細胞を含む骨ライニング細胞 (BLC) で構成されます。
研究の内容と成果
急性骨髄性白血病マウスモデルを用いた解析から、白血病幹細胞の重要なサブセットである L-GMP*11は、骨内膜領域では G0 期 (静止期) に留まる割合が高いことが確認されました。骨内膜 L-GMP では細胞周期阻害因子である p21 および p57 の発現増加が確認されました。免疫蛍光イメージングにより、静止期の白血病細胞が骨内膜領域、特に Alcam+ BLC が豊富な領域に集中しており、それらの多くが直接接着していることが確認されました。逆に、 Alcam+ BLC が少ない領域では、増殖期の白血病細胞が多く見られました。これらの結果は、骨内膜ニッチにおける Alcam+ BLC が、白血病幹細胞の静止状態維持に重要な役割を果たしていることを強く示唆しています。
白血病の進行に伴うニッチ構成要素の動態を解析した結果、血管性ニッチを代表する CD51+ CD140a+ 間葉系幹細胞の数が白血病進行に伴い有意に増加しました。対照的に、骨内膜領域の Alcam+ BLC の数は白血病進行に伴い減少しました。この Alcam+ BLC の減少は、骨内膜における Ki67−白血病細胞 (静止期細胞) の割合の減少と一致しており、Alcam+ BLC の減少による骨内膜ニッチによるサポートの喪失が白血病幹細胞の活性化につながる可能性を示唆しています。一方、白血病進行期の血管性ニッチにおける CD51+ CD140a+ 間葉系幹細胞の増加は、CD51+ CD140a+ 間葉系幹細胞が分泌するサイトカインや細胞増殖因子などの液性因子により白血病細胞の増殖を支持していると考えられました。
Transwell インサートを用いた Alcam+ BLC と L-GMP の共培養実験から、ニッチ細胞表面への接着が白血病幹細胞の維持に重要であることが明らかとなりました。Alcam+ BLC は、HSC や急性リンパ性白血病 (ALL) 細胞を骨内膜領域に接着させることで静止状態を維持する骨形成因子であるオステオポンチン (OPN) を豊富に分泌しています。白血病モデルマウスでは、Alcam+ BLC は CD51+ CD140a+ 間葉系幹細胞と比較してオステオポンチン mRNA の発現が高く、白血病進行に伴い Alcam+ BLC におけるオステオポンチン mRNA 発現が増加することが明らかとなりました。免疫蛍光イメージングにより、Alcam+ BLC 表面に高いオステオポンチン発現が確認され、Ki67− 白血病細胞がこれらのオステオポンチンに富む細胞の周囲に集積していることが確認されました。
さらに、本研究グループは Transforming Growth Factor-β1 (TGF-β1) が Alcam+ BLC におけるオステオポンチン発現の制御因子として関与していることを明らかにしました。骨内膜周囲の L-GMP は、骨髄中央部の L-GMP と比較して高いレベルの TGF-β1 mRNA を発現していました。また、白血病が進行するにつれて、Alcam+ BLC におけるTGF-β 受容体2 (Tgfbr2) mRNA の発現と、TGF-β 経路の主要なシグナル伝達因子であるリン酸化 Smad2/3 の割合が有意に上昇していました。Alcam+ BLC は TGF-β1 の刺激によりオステオポンチンおよび Tgfbr2 mRNA の発現を誘導することを確認しました。これらのデータは、白血病幹細胞から分泌された TGF-β1 が Alcam+ BLC のオステオポンチン産生を促進するというメカニズムが存在していることを示唆しています。分泌されたオステオポンチンは白血病幹細胞を骨内膜領域に留め、静止状態に維持しています。
本研究では、白血病幹細胞の維持と白血病の進行における骨内膜ニッチと血管性ニッチの果たす役割の違いを明らかにしました。特に、白血病幹細胞の静止状態は Alcam+ BLC との密接な接触によって維持されており、Alcam+ BLCの存在が白血病再発の原因の一つであると考えられました。また、白血病の進行に伴い、血管性ニッチではCD51+ CD140a+ 間葉系幹細胞が増加し、白血病幹細胞の活性化と増殖を支持しています。本研究ではさらに、骨内膜における白血病幹細胞と Alcam+ BLC 間のクロストークを仲介する TGF-β1/Tgfbr2/OPN シグナル経路を明らかにしました。
今後の展開
TGF-β1/Tgfbr2/OPN シグナル経路の阻害は、白血病幹細胞からの TGF-β1 分泌抑制、Alcam+ BLC における TGF-β 受容体の不活性化、Alcam+ BLC からのオステオポンチン産生阻害、あるいは白血病幹細胞のオステオポンチン受容体の遮断を通じて、白血病幹細胞のニッチへの接着や静止状態の維持を妨げる可能性があります。これらの知見から、従来の化学療法では排除が困難であった静止期白血病幹細胞を標的とした治療薬開発が可能となり、白血病治療効果の向上と再発率の低減が期待されます。本研究の成果は、白血病再発に対する新規治療法開発の基盤として重要な意義を持つものです。
用語解説
- (※1) Alcam (Activated Leukocyte Cell Adhesion Molecule、別名 CD166)
- 免疫グロブリンスーパーファミリーに属するI型膜貫通型接着分子で、細胞間接着や細胞移動の調節に関与している。
- (※2) 骨ライニング細胞 (bone lining cell, BLC)
- 骨表面を覆う細胞集団で、骨芽細胞や骨芽細胞前駆細胞、間葉系幹細胞から構成されている。
- (※3) 白血病幹細胞 (leukemia stem cell, LSC)
- 白血病細胞を生み出す元となる細胞。
- (※4) Transforming Growth Factor-β1 (TGF-β1)
- TGF-βスーパーファミリーに属するサイトカインで、細胞の成長、分化、増殖、アポトーシスや免疫応答、組織の線維化など多様な細胞機能を制御する重要な分泌タンパク質。
- (※5) TGF-β受容体2 (TGF-β receptor 2, Tgfbr2)
- 細胞膜上に存在するセリン/スレオニンキナーゼ活性を持つ受容体で、TGF-β リガンドと結合した後に TGF-β 受容体1をリン酸化して活性化し、細胞内のシグナル伝達を開始する役割を担っている。
- (※6) オステオポンチン (Osteopontin, OPN)
- オステオポンチンは、細胞外マトリックスタンパク質の一種で、免疫機能の調節、細胞接着の促進、炎症反応の制御、創傷治癒の促進など、多様な生理機能に関与している。
- (※7) 急性骨髄性白血病 (acute myeloid leukemia, AML)
- 骨髄系細胞ががん化し、白血病細胞が異常増殖する疾患。
- (※8) 完全寛解
- 治療後、白血病による症状や検査での異常が見られなくなり、正常な造血機能が回復した状態。
- (※9) 造血幹細胞 (hematopoietic stem cell, HSC)
- 血液細胞を作る元になる細胞。
- (※10) 間葉系幹細胞 (mesenchymal stem cell, MSC)
- 骨、軟骨、脂肪などへの分化能を持つ組織幹細胞。
- (※11) L-GMP (leukemia granulocyte-macrophage progenitor)
- 顆粒球マクロファージ前駆細胞 (granulocyte-monocyte progenitor, GMP) と類似した特徴を持ち、白血病幹細胞を多く含む白血病細胞。
謝辞
本研究は科学研究費助成事業 (22K08478, 23H02935, 23K18301) および化学及血清療法研究所の助成を受けたものです。
論文情報
- 掲載誌:
- Leukemia
- タイトル:
- Acute Myeloid Leukemia Stem Cells Remodel the Bone Marrow Niche via TGF-β-Activated Alcam+ Bone Lining Cells, Creating a Self-Sustaining Environment
- 著者名:
- Ngan Thi Kim Nguyen¹、Hisayuki Yao¹、Kentaro Hosokawa¹、Yuki Esaki¹、Ryosuke Yuta¹、Shunichi Adachi¹、Fumio Arai¹*
1九州大学 大学院医学研究院 応用幹細胞医科学部門 幹細胞再生修復医学分野/がん幹細胞医学分野
*責任著者:新井 文用 - DOI:
- 10.1038/s41375-025-02640-4
お問合せ先
九州大学 大学院医学研究院 応用幹細胞医科学部門 幹細胞再生修復医学分野/がん幹細胞医学分野
教授 新井 文用 (アライ フミオ)
092-642-4834 092-642-4835 arai.fumio.603(at)m.kyushu-u.ac.jp

