2026.04.30
命の始まりは父母ゲノムの「別居」から -父母ゲノム間の競合が受精卵の発生を助ける-(先端医療医学講座 原田 哲仁教授)
理化学研究所(理研)生命機能科学研究センター染色体分配研究チームの京極博久客員研究員(神戸大学大学院農学研究科准教授)、北島智也チームディレクター、フィジカルバイオロジー研究チームの柴田達夫チームディレクター、無細胞タンパク質合成研究チームの清水義宏チームディレクター、生命医科学研究センター疾患エピゲノム遺伝研究チームの井上梓チームディレクター、九州大学大学院医学研究院の原田哲仁教授らの共同研究グループは、受精卵[1]において母と父のゲノム[2]が二つの前核[3]に分かれて「別居」することが、その後の正常な胚発生に重要であることを発見しました。
本研究成果は、生命の最初期における発生の仕組みの理解を深めるとともに、不妊治療における受精卵の発生能力の理解に貢献すると期待されます。
哺乳類の受精卵では、雌性前核と雄性前核という二つの核が形成され、母親由来と父親由来のゲノムが最初の細胞分裂まで別々に保持されます。しかし、父母ゲノムが離れて存在する生物学的意義は明らかではありませんでした。
共同研究グループはマウスを用いて、父母ゲノムを人工的に一つの前核にまとめた受精卵を作製しました。この父母同居型の前核はサイズが巨大化する一方で、ゲノムのヒストン修飾[4]レベルが全体的に低下し、その後の胚発生能力も低下することが分かりました。さらに前核のサイズを制御する因子は細胞質中に存在し、二つの前核はこの因子を奪い合うことでお互いの部屋をコンパクトに抑え、自身のヒストン修飾を維持しやすくすることが明らかになりました。
本研究は、科学雑誌『Nature』オンライン版(4月29日付:日本時間4月30日)に掲載されました。

父母ゲノム別居による胚発生制御
哺乳類の生命は、卵子と精子が受精して生じる一つの受精卵から始まります。この受精卵中では、母親由来と父親由来のゲノム(父母ゲノム)がそれぞれ別々の核(前核)に分かれて別居した状態になっています。この別居状態は受精卵が最初の細胞分裂を行うまで保持され、2細胞期以降になると一つの核に父母ゲノムが同居する通常の状態となります。
このように二つの前核という部屋を形成することは、多核細胞という不安定な状態を伴うにもかかわらず、哺乳類の受精卵に広く共通する現象です。しかし、なぜ父母ゲノムが同じ部屋に同居せず、あえて別々の部屋に分かれて存在する一方で、生殖補助医療の現場では、父母ゲノムが一つの前核に同居した受精卵(1前核受精卵)が観察されることがあり、その発生特性については十分に理解されていません。
これまでの研究から、受精卵では母と父のゲノムが異なるヒストン修飾状態を持ち、発生の初期段階で大きく変化することが発生に必須であることが知られています注)。一方で、父母ゲノムの空間的な分離や前核の大きさそのものが、ヒストン修飾や胚発生にどのように関与しているのかは、実験的に検証されていませんでした。
そこで本研究では、受精卵において父母ゲノムが二つの前核に別居することの生物学的な意義を明らかにすることを目的として、その仕組みと胚発生への影響を解析しました。
注)Eckersley-Maslin, M. A., Alda-Catalinas, C. & Reik, W. Dynamics of the epigenetic landscape during the maternal-to-zygotic transition. Nat. Rev. Mol. Cell Biol. 19, 436–450 (2018)
共同研究グループはまず、マウスの卵子と精子を用いて、父母ゲノムが一つの前核に同居する受精卵(1前核受精卵)を人工的に作製し、通常のように父母ゲノムが二つの前核という別々の部屋に分かれている受精卵(2前核受精卵)と比較しました(図1a)。
3次元画像解析[5]を用いて前核の体積を定量的に測定したところ、1前核受精卵では、通常の受精卵における雌性前核と雄性前核の体積の合計とほぼ同程度の大きな部屋(前核)が形成されていることが分かりました(図1b中央)。
次にヒストン修飾の状態を解析した結果、1前核受精卵ではヒストン修飾レベルが全体的に低下していることが明らかになりました(図1b右)。この結果は、核の大きさがヒストン修飾レベルの維持に影響する可能性を示唆しています。

図1 父母同居型受精卵で形成される大きな前核とヒストン修飾の低下
a)顕微操作技術を用いた2前核受精卵と1前核受精卵の作成の様子。父ゲノムを母ゲノムの近くに注入することで作製する。
b)通常の受精卵(2前核受精卵)では、母ゲノム(マゼンタ)と父ゲノム(グリーン)が別々の前核(部屋)として形成される。父母ゲノムが一つの前核に同居する受精卵(1前核受精卵)では、二つ分に相当する大きさの前核が形成されたが、それぞれのゲノムがほとんど混じり合わず別々の半球状に分布していた。また、1前核受精卵では父母ゲノムのヒストン修飾レベル(H3K4me3)が全体的に低下していた。カラー写真は、ヒストン修飾レベル(H3K4me3)の強さを示しており、暖色ほどシグナルが強く、寒色ほど弱いことを示す。スケールバーは5マイクロメートル(μm、1μmは100万分の1メートル)
共同研究グループは、前核サイズがどのように制御されているのかを検証しました。母性ゲノムのみ、あるいは父性ゲノムのみの前核を一つ持つ受精卵を作製して解析したところ、いずれの場合も前核サイズは通常より大きくなりました(図2a)。この結果は、前核サイズを決める要因が父母ゲノムのどちらか固有のものではなく、細胞質に含まれる何らかの因子が前核に作用していることを示唆しています。そこで、細胞質の量を半分または倍に操作する実験を行い、前核サイズへの影響を調べました(図2b)。その結果、前核サイズは細胞質の量に応じて変化し、細胞質量を減らすと前核は小さくなり、細胞質量を増やすと前核は大きくなりました(図2c)。これらの結果から、細胞質中の因子の量には限りがあり、前核はこの因子を取り込みながら成長し、その量によってサイズが制限されていることが示されました。
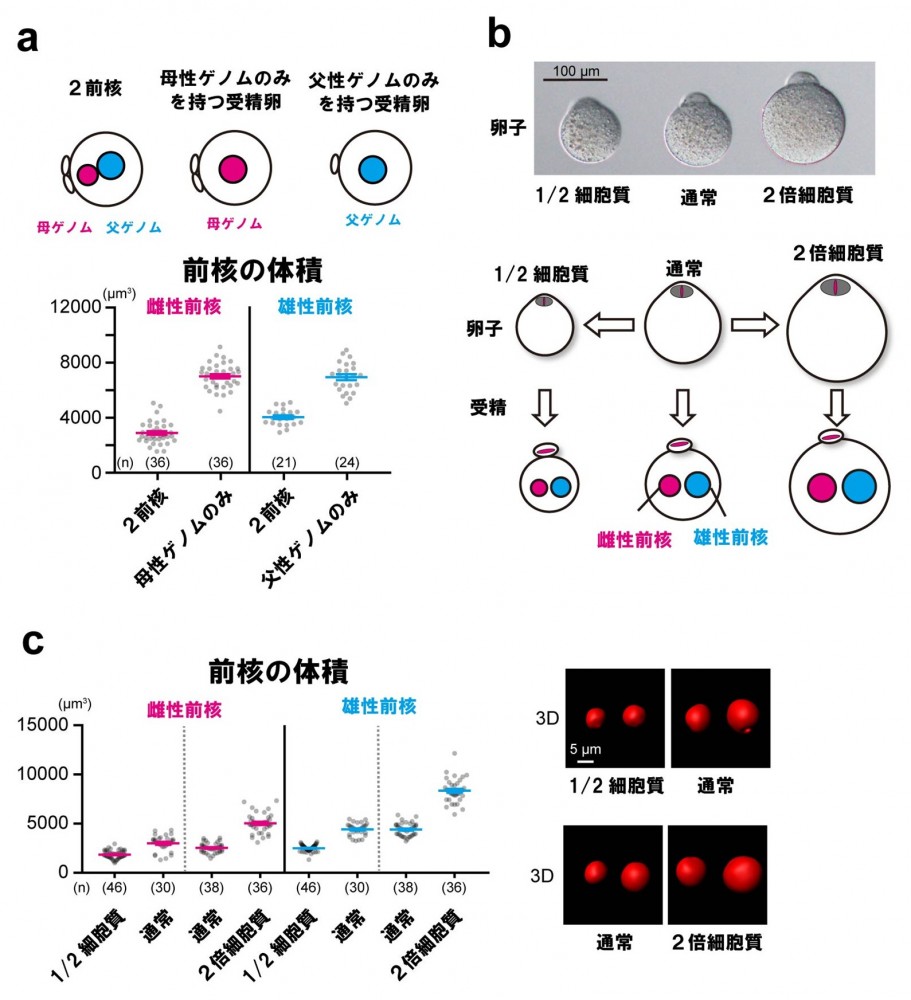
図2 前核サイズを制限する細胞質因子
a)母性ゲノムのみ、または父性ゲノムのみを持つ受精卵は、2前核受精卵よりも大きな前核を形成した。
b)顕微操作により細胞質量を半減もしくは倍加させた卵子を作製した後に受精させ細胞質量が異なる受精卵を作製。
c)細胞質量を操作すると、前核サイズもそれに応じて変化した。グラフ横の画像は、3次元画像解析で再構成した前核。グラフ横軸の(n)は観察した受精卵の数を示す。
次に共同研究グループは、父母ゲノムの前核のサイズがどのようにして決まっているのかを調べました。核は核膜[6]によって細胞質から隔てられていますが、核膜に開いた小孔(核膜孔[6])を介して核内外の物質輸送が行われます。核膜孔の構成成分の集積と核内輸送速度を解析したところ、雄性前核では核膜孔がより多く形成され、核内への物質取り込み速度が雌性前核よりも速いことが分かりました(図3a)。これらの結果を基に、前核のサイズを決定する要因として、1)二つの前核は細胞質中の有限な因子を取り合いながら成長し、2)核膜孔密度の差によって取り込み能力が異なるため、競合の結果として前核サイズが決まるという二つの仮定を設定し、これに基づいた数理モデルを構築しました。このモデルで前核成長の時間変化を予測したところ、雄性前核は雌性前核よりもサイズの成長速度が速いことなど、実際に観察された現象を再現できました(図3b)。
さらに解析の結果、前核サイズの変化とヒストン修飾レベルの間には逆相関があることが明らかになりました。すなわち、前核が大きくなるほどヒストン修飾レベルが低下し、前核サイズが適切に制限されるとヒストン修飾レベルが維持されることが分かりました(図3c)。
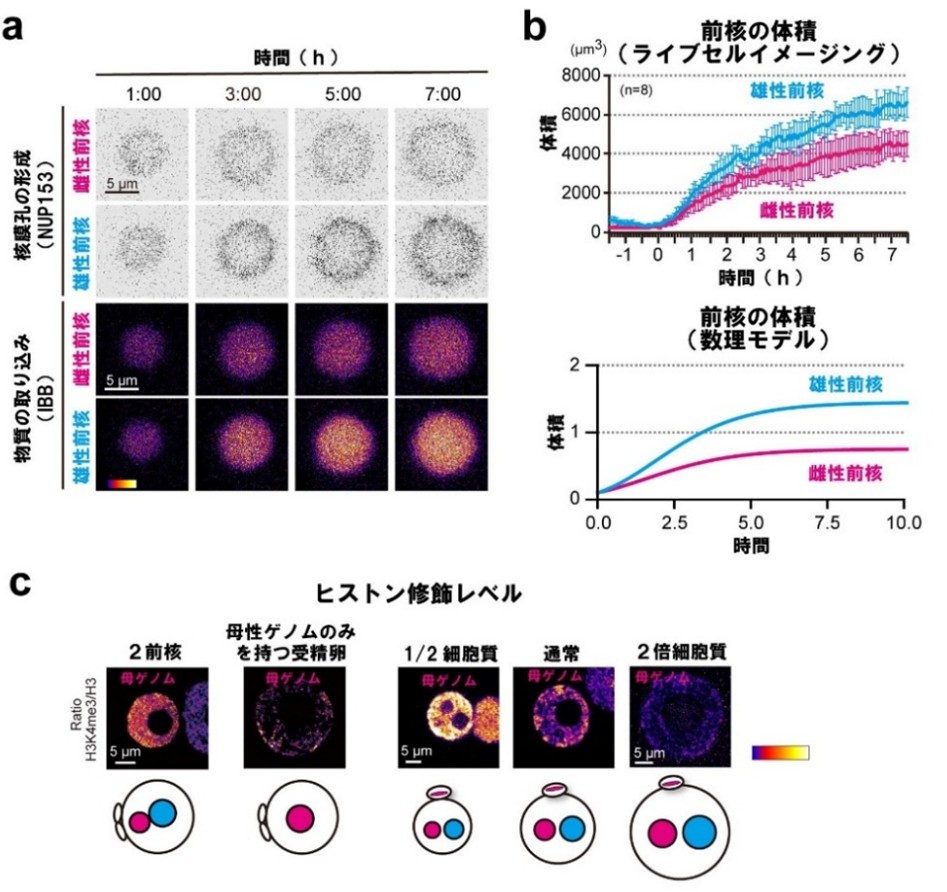
図3 核膜孔密度の差による前核サイズ競合
a)ライブセルイメージング(生細胞イメージング)による核膜孔の形成と核内への物質取り込み速度の計測。雄性前核では核膜孔の形成と核内への物質取り込みが雌性前核より速かった。
b)数理モデルでも、この競合による前核成長の過程が再現された。
c)前核サイズとヒストン修飾レベルの関係。前核が大きくなるほどヒストン修飾レベルが低下していた(ヒストン修飾レベルの表現は図1bを参照)。
最後に共同研究グループは、1前核受精卵が正常に発生して仔(子)マウスとなるかを検証しました。その結果、1前核受精卵は通常の2前核受精卵と比べて出生に至る割合(産仔率)が低下しました。さらに、この低下が回復可能かを調べるため、第二の前核を一時的に導入して2核の競合状態をつくると、前核サイズが抑えられ、低下していたヒストン修飾が回復し、産仔率も改善しました(図4a、b)。
また、ヒストン修飾レベルを増やす薬剤(Trichostatin A:TSA[7])処理や遺伝子発現操作(Kdm5b KD[8])によっても、発生率は部分的に回復しました(図4c)。

図4 競合回復によるヒストン修飾と産仔率の回復
a)1前核受精卵に第二の前核が一時的に導入された状態(P1PN)。前核サイズが抑制され、ヒストン修飾が回復していた(ヒストン修飾レベルの表現は図1bを参照)。
b)競合回復による産仔率の回復。1前核受精卵で低下した産仔率は、競合回復により上昇した。
c)ヒストン修飾を増やす薬剤(Trichostatin A:TSA)処理や、ヒストン修飾を低下させる酵素(Kdm5b)の発現阻害(KD)操作(Kdm5b KD)により、産仔率は部分的に回復した。
以上の結果から、受精卵では父母ゲノムが二つの前核という別々の部屋に分かれて存在するため、細胞質中の限られた因子を巡る前核同士の競合が生じ、前核サイズが適切に制御されることが明らかになりました。このサイズ制御によってヒストン修飾レベルが維持され、その後の胚発生能力が支えられていると考えられます。すなわち、父母ゲノムが別々の部屋に「別居」するという受精卵の特徴的な構造は、ヒストン修飾レベルを安定に保ち正常な発生を可能にするための基本的な仕組みであることが示されました。これまで前核の分離は受精に伴う構造的特徴と考えられてきましたが、本研究により、その空間的分離自体が発生制御に重要な役割を果たしていることが明らかになりました。
本成果は、生命の最初期における発生原理の理解を大きく前進させるものです。特に、前核サイズ制御とヒストン修飾の変化が関連していることを示した点は、初期胚における核サイズ制御の新たな概念を提示するものです。
また、不妊治療の現場では1前核受精卵が一定割合で観察され、それらが臨床的に利用される場合もあります。本研究は、1前核受精卵の発生特性に関する基礎的知見を提供するものであり、受精卵評価の科学的基盤の構築に貢献すると期待されます。ただし、本研究はマウスを用いた基礎研究であり、ヒト受精卵への直接的な適用には慎重な検討が必要です。
今後は、ヒトを含む他の哺乳類において同様の競合機構が存在するかを明らかにするとともに、前核サイズ制御とヒストン修飾の関係を含めた分子機構の解明を進める必要があります。ヒストン修飾の変化は重要な要因の一つと考えられますが、胚発生に影響を与える仕組みの全体像の解明が今後の課題です。
- 掲載誌:
- Nature
- タイトル:
- Cytoplasmic competition between separate parental pronuclei in zygotes
- 著者名:
- Hirohisa Kyogoku, Mitsusuke Tarama, Masahiro Matsuwaka, Tappei Mishina, Akihito Harada, Reiko Nakagawa, Mami Kumon, Yoshihiro Shimizu, Yasuyuki Ohkawa, Tatsuo Shibata, Azusa Inoue, Tomoya S Kitajima
- DOI:
- 10.1038/d41586-026-01270-9
- [1] 受精卵
- 卵子と精子が受精して形成される、発生の最初の細胞である。哺乳類では受精直後、母親由来と父親由来のゲノム([2]参照)はそれぞれ別々の核(前核([3]参照))に収納される。この二つの前核は、最初の細胞分裂の直前まで分かれた状態で存在する。
- [2] ゲノム
- 生物の染色体に含まれる全遺伝情報。物質的実体であるゲノムDNAは、真核細胞ではヒストンタンパク質などと結合した染色体として存在する。
- [3] 前核
- 受精により精子が卵子に入ると、卵子の中に卵子由来の核と精子由来の核の二つが観察される。これらを前核と呼ぶ。
- [4] ヒストン修飾
- DNAはヒストンというタンパク質に巻き付いて核内に収納されている。ヒストンに化学修飾が付加されることで、遺伝子の働きやクロマチンの状態が調節される。この修飾状態は、初期胚発生における遺伝子発現制御に重要な役割を持つ。
- [5] 3次元画像解析
- 顕微鏡観察で得られた2次元画像から、外形を立体的に再構成する画像解析法。
- [6] 核膜、核膜孔
- 核膜とは、核を覆う二重の脂質膜。核膜孔とは、核膜に存在するタンパク質複合体であり、核と細胞質の間で分子を輸送する通路として働く。タンパク質やRNAなどの分子は核膜孔を通って核内に取り込まれるため、その数や密度は核内への物質取り込み能力に影響する。
- [7] Trichostatin A:TSA
- Trichostatin A(トリコスタチンA)は、ヒストン脱アセチル化酵素(HDAC)を阻害する薬剤。ヒストン修飾状態を変化させる作用を持ち、細胞の遺伝子発現やクロマチン構造に影響を与える。本研究では、ヒストン修飾を増加させる目的で用いた。
- [8] Kdm5b KD
- Kdm5bはヒストンH3K4me3修飾を除去する酵素(ヒストン脱メチル化酵素)。KDは「ノックダウン(knockdown)」を意味し、遺伝子の働きを部分的に抑える操作を指す。本研究ではKdm5bを抑制することでH3K4me3修飾量を増加させる操作を行った。
本研究は、理化学研究所運営費交付金(生命機能科学研究、理研新領域開拓課題「長時間分子生物学(領域代表者:北島智也)」)で実施し、文部科学省科学研究費助成事業学術変革領域研究(A)「動的な生殖ライフスパン:変動する生殖細胞の機能と次世代へのリスク(領域代表者:北島智也、JP23H04947)」「細胞競合における細胞間相互作用を計測するための空間オミクス技術開発(研究代表者:原田哲仁、JP21H05292)」「エピゲノムによる発生保証機構(研究代表者:井上梓、JP25H01355)」、同学術変革領域研究(B)「初期胚が持つ染色体分配異常へのリスクマネジメント(研究代表者:京極博久、JP25H01445)」、同新学術領域研究(研究領域提案型)「染色体イメージングによる卵子インテグリティの予見(研究代表者:北島智也、JP18H05549)」「核サイズに制御された全能性獲得メカニズムの解明(研究代表者:京極博久、JP20H05376)」「受精卵が全能性を維持するために染色体分配異常から回復するメカニズムの解明(研究代表者:京極博久、JP22H04674)」「全能性獲得機構の解明のためのmulti-omics技術の開発(研究代表者:原田哲仁、JP20H05368)」「細胞核・クロマチン構造のダイナミクスと遺伝子制御(研究代表者:木村宏、JP18H05527)」「空間マルチオミクスでアプローチする初期胚における細胞運命決定機序の理解(研究代表者:大川恭行、JP22H04676)」、日本学術振興会(JSPS)科学研究費助成事業基盤研究(A)「人工動原体の構築による染色体分配の機構の解明(研究代表者:北島智也、JP25H00981)」「全細胞オミクスによる骨格筋組織を構築するシステムの解明(研究代表者:大川恭行、JP20H00456)」、同基盤研究(B)「哺乳類卵母細胞における紡錘体二極化の機構の解明(領域代表者:北島智也、JP21H02407)」、同若手研究「細胞の自律運動と協同的集団運動のアクティブマター物理学(研究代表者:多羅間充輔、JP19K14673)」、科学技術振興機構(JST)戦略的創造研究推進事業さきがけ「顕微操作技術による初期胚の不安定なゲノムの分配システムの解明(研究代表者:京極博久、JPMJPR20K4)」「組織特異的ゲノム構造の再構築技術の開発(研究代表者:原田哲仁、JPMJPR19K7)」、同創発的研究支援事業「初期胚が持つ特殊な複製様式の意義とメカニズムの解明(研究代表者:京極博久、JPMJFR2338)」「ヒストン修飾を基軸とした卵子プログラミング仮説の検証(研究代表者:井上梓、JPMJFR2335)」、日本医療研究開発機構(AMED)BINDS(JP22ama121017)、文部科学省共同利用・共同研究システム形成事業「学際領域展開ハブ形成プログラム(JPMXP1323015486)」の助成を受けて行われました。
また、松若正篤は、理化学研究所の大学院生リサーチ・アソシエイト(JRA)制度の支援を受け、研究を遂行しました。

